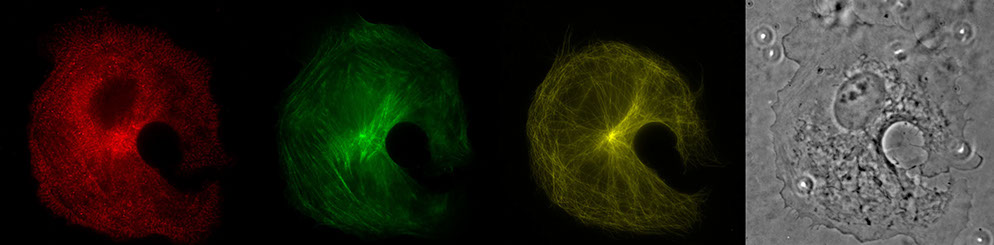
Исследования
Группа профессора Г.Е. Онищенко
Общая тема «Механизмы выживания и гибели клеток»
1. Механизмы гибели и устойчивости опухолевых и нормальных клеток при действии ряда химиотерапевтических препаратов.
Одной из проблем современной клеточной биологии является определение типа клеточной гибели и механизмов каждого из типов при действии химиотерапевтических препаратов. Если в течение длительного времени основным типом считали апоптоз, затем выделили до 15 типов клеточной гибели, то в настоящее время нередко отсутствует точная классификация гибели клетки при действии того или иного препарата и используется термин просто «клеточная смерть (cell death)». Однако выявление точных признаков клеточной гибели опухолевых клеток позволяет определить мишени в каждом конкретном случае, а для нормальных клеток определить потенциальные побочные эффекты, что позволит разработать в том числе и протекторные подходы.
Так как процессы аутофагии в одних случаях играют протекторную роль, в других участвуют в реализации программы клеточной гибели, в настоящей время группой проводятся исследования роли аутофагических процессов в клетках эпидермального происхождения при запуске апоптоза воздействием агентов, повреждающих ДНК, стабилизирующих или разрушающих микротрубочки или индукторов стресса ЭПР, которые уже используют в качестве химиотерапевтических препаратов (доксорубицин, паклатаксел, бортезомиб) или рассматривают как потенциальные препараты (туникамицин, сукцинат витамина Е).
Выживание опухолевых клеток, которое может приводить к рецидиву роста опухоли, является ещё одной проблемой химиотерапии. Выжившие клетки, после удаления химиотерапевтических препаратов могут переходить в состояние старения (терапия-индуцированное старение), дифференцировки, полиплоидизироваться, формировать микроядра. При восстановлении пролиферативной активности такие клетки образуют новую популяцию, генетически и, возможно, функционально отличающуюся от исходной. В настоящее время мы изучаем функциональных свойств устойчивых к действию доксорубицина, бортезомиба и туникаамицина клеток. Проводятся исследования пролиферативного и дифференцировочного потенциалов, признаков старение, уровня подвижность (способность к метастазированию). Также ведётся исследование морфологических и функциональных характеристик биосинтетического (эндоплазматический ретикулум, аппарат Гольджи, лизосомы и аутофагосомы) и митохондриального компартментов. Результаты такого исследования помогут оценить туморогенность новой популяции клеток и в дальнейшем выбрать стратегию последующей терапии.
Состав подгруппы: проф., Онищенко Галина Евгеньевна, член-кор., проф. д.б.н., член-корр. РАН Воротеляк Екатерина. Андреевна, доц. д.б.н.Мария Владиславовна Ерохина, доц. д.б.н. Николай Константинович Исаев, доц. к.б.н. Ольга Петровна Кисурина-Евгеньева, ст.н.с. к.б.н. Марина Ильинична Мурашева, асс. к.б.н. М.А. Савицкая Маргарита Анатольевна,уч. маст. Илья Игоревич Захаров.
Контакты сотрудников: доц. к.б.н. Кисурина-Евгеньева Ольга Петровна evgengeva@mail.ru
2. Изучение влияния фитогормонов и растительных экстрактов на культивируемые нормальные и опухолевые клетки человека различного тканевого происхождения.
Поиск и тестирование природных соединений, оказывающих как положительное, так и отрицательное действие на организм человека и животных, постоянно расширяются. Наши исследования направлены на изучение конкретных клеточных механизмов, которые могут являться мишенями для действия многих природных соединений. Мы полагаем, что в результате работы будут разработаны тест-системы для испытания действия широкого спектра разных агентов на физиологию клеток эпидермиса и соединительной ткани. Оценка с помощью МТТ-теста жизнеспособности культивируемых нормальных и опухолевых клеток человека HNEK, DU145, hASC, HaCaT и A431 при действии экстрактов Duranta erecta Linn., полученных из листьев и каллусных культур, позволяет определить действующие концентрации экстрактов и сравнить эффективность их действия на исследуемые нормальные и опухолевые клетки различного тканевого происхождения.
Ранее было показано, что фитогормон абсцизовая кислота усиливает дифференцировку в 2D-клеточных линиях, включая иммортализованные кератиноциты человека (НаСаТ). Оценка влияния абсцизовой кислоты на распределение маркеров дифференцировки кератиноцитов в 3D-моделях кожи человека (сфероидах, состоящих из смеси фибробластов и кератиноцитов; кожных эквивалентах, включающих слой фибробластов в коллагеновом матриксе и поверхностный слой кератиноцитов) позволит определить, влияет ли абсцизовая кислота на распределение маркеров дифференцировки в более сложных моделях кожи человека. Данные проекта позволят определить, могут ли используемые модели применяться в качестве тест-систем для исследования свойств широкого спектра агентов, потенциально влияющих на дифференцировку клеток кожи.
В рамках данной подтемы также ведутся исследования, оценивающие влияние абсцизовой и гибберелиновой кислот на уровень синтеза белков внеклеточного матрикса проколлагена I и фибронектина клетками фибросаркомы человека линии НТ1080. С помощью вестерн-блоттинга удастся определить, стимулируют ли данные фитогормоны синтез проколлагена I клетками фибросаркомы НТ1080, не синтезирующими этот белок в стандартных условиях культивирования, а также влияют ли растительные гормоны на синтез фибронектина. Анализ влияния абсцизовой кислоты на уровень синтеза маркера стресса ЭПР GRP78 клетками фибросаркомы человека линии НТ1080 с помощью вестерн-блоттинга позволит определить, связано ли обнаруженное нами раннее перераспределение маркера стресса ЭПР GRP78 в клетках фибросаркомы с повышением уровня синтеза этого белка.
Состав подгруппы: проф. Смирнова Елена Александровна, доц. к.б.н. Мария Сергеевна Вильданова, м.н.с. к.б.н. Екатерина Павловна Турищева, уч. маст. Илья Игоревич Захаров
Контакты сотрудников: доц. к.б.н. Мария Сергеевна Вильданова vch41048@mail.ru
3. Разработка методов идентификации различных штаммов микобактерий туберкулёза в макрофагах человека
Ранее проведённые исследования и данные литературы показывают, что направление активации макрофагов – по пути про- или противовоспалительного фенотипа (М1 и М2, соответственно) – является вопросом особой важности при реализации своей стратегии выживания в макрофагах человека для внутриклеточных микобактерий туберкулёза. Известно, что в М2-макрофагах возбудитель туберкулёза имеет более высокие шансы для выживания и дальнейшего персистирования. Ранее была проведена разработка модели инфицирования провоспалительных макрофагов (М1) человека микобактериями туберкулёза (штамм BCG) и методики выявления живых и мертвых бактерий методом флуоресцентной микроскопии. Целью настоящего исследования является отработать идентификацию микобактерий туберкулёза (штамм H37Rv) в провоспалительных макрофагах методом электронной микроскопии при разных условиях воздействия. Будет создана и отработана методика идентификации микобактерий туберкулёза внутри макрофагов после воздействия разных форм противотуберкулёзных препаратов и проведена оценка их влияния на дифференцировочный статус провоспалительных макрофагов. Будет отработана методика электронно-микроскопической идентификации внутри макрофагов микобактерий туберкулёза, в том числе при разных условиях воздействия на них разных форм противотуберкулёзных препаратов.
Состав подгруппы: доц. д.б.н. Мария Владиславовна Ерохина., с.н.с. к.б.н. Александр Георгиевич Масютин
Контакты сотрудников: доц. д.б.н.Мария Владиславовна Ерохина erokhinam@bk.ru
4. Изучение структуры, локализации и процессов биодеградации углеродосодержащих наночастиц в клетках различных органов млекопитающих.
Вопросы изучения реакции клеток млекопитающих на присутствие таких наночастиц остаются крайне актуальными актуальными в рамках общей проблемы нанобиобезопасности. Планируется продолжение анализа накопления МУНТ в клетках ЖКТ мыши и процессов их биодеградации под действием активных веществ желудка и кишечника. Работу планируется проводить на ранее зафиксированных для электронной микроскопии кусочках желудка, а также дистальных отделов подвздошной и ободочной кишки мышей, получавших суспензию промышленных МУНТ с питьевой водой. В ходе ультраструктурного исследования гистологического материала ЖКТ мышей (желудка и, подвздошной и ободочной кишки) методами аналитической электронной микроскопии (дифракции электронов, и энергодисперсионной рентгеновской спектрометрии) будет продолжен поиск и идентификация МУНТ или продуктов их биодеградации в клетках и тканях. На основе полученных данных будет проведена оценка накопления наноматериала в органах ЖКТ экспериментальных животных при пероральном введении. Методами ультраструктурного анализа и аналитической электронной микроскопии будет произведено сравнение направления и интенсивности деградации МУНТ после прохождения полного пищеварительного цикла in vivo и с аналогичными процессами под действием желудочного сока мыши и соляной кислоты in vitro. Для сравнения процессов биодеградации МУНТ под действием активных веществ желудочно-кишечного тракта, будут использованы МУНТ, прошедшие полный пищеварительный цикл, а также МУНТ, проинкубированные с желудочным соком мыши или соляной кислотой. В ходе исследования будет продемонстрировано, какие морфологические изменения происходят с МУНТ при пероральном введении мышам, и в каких отделах ЖКТ. Также планируется выявить продукты биотрансформации МУНТ в клетках органов ЖКТ и провести их идентификацию. Данные по морфологии МУНТ, выделенных из ЖКТ, будут сопоставлены с результатами, полученными in vitro, при инкубации с активными веществами желудка. Это даст ответ на вопрос, как именно идет биодеградация МУНТ в ЖКТ, и насколько эффективно.
Состав подгруппы: доц. д.б.н.Мария Владиславовна Ерохина., с.н.с. к.б.н. Александр Георгиевич Масютин
Контакты сотрудников: с.н.с. к.б.н. Александр Георгиевич Масютин squiggoth@yandex.ru
5. Влияние высокотоксических металлосодержащих и органических соединений.
В проекте проводятся исследования влияния ионов кадмия на жизнеспособность культивированных астроцитов. Ожидается, что добавление хлорида кадмия в миллимолярных концентрациях вызывает гибель культивированных астроцитов и при этом на промежуточном этапе развития повреждения клеток происходит изменение размера ядрышек. Морфология и активность ядрышек очень чувствительны к сигналам повреждения, которые в совокупности входят в активно развивающуюся концепцию ядрышкового стресса. Ядрышковый стресс отражает нарушение функции ядрышка, вызванное сбоем в биогенезе рибосом и дефектной архитектурой ядрышка. Важно отметить, что изменения в ядрышках являются характерной чертой многих патологий человека, однако, прямое токсическое действие ионов кадмия на ядрышки астроцитов в настоящее время мало исследовано. Мы изучаем возможность использования размеров ядрышка в качестве тест-системы для оценки уровня жизнеспособности астроцитов при действии токсических соединений.
Состав подгруппы: доц. д.б.н. Николай Константинович Исаев, Стрижкова А.Б.
Контакты сотрудников: доц. д.б.н. Николай Константинович Исаев nisaev61@mail.ru
6. Подгруппа Васильевой Т.В.
Научная группа занимается исследованиями тканей с применением традиционных гистологических и иммуногистохимических методов. Помимо методов пробоподготовки и анализа образцов тканей группа применяет в ходе выполнения научных задач экспериментальные in vivo модели воспалительных и аллергических реакций, такие как индуцированное воспаление в воздушном мешке, декстрасульфатная модель колита, овальбумин индуцированный кожный дерматит и т.д. Отработка и валидация необходимых для исследования животных моделей является важной частью деятельности группы.
Большая часть деятельности группы связано с изучением регуляции воспалительных и аллергических процессов в организме, роли состояния митохондрий, различных внутриклеточных факторов и функциональной активности ткани на развитие и протекание воспалительных процессов. В частности в ходе работы было показано, что митохондриально накапливающиеся соединения различного механизма действия могут понижать интенсивность протекания воспалительных реакций, особенно на стадии экссудации, что сокращает общую продолжительность воспалительного процесса и позволяет организму раньше осуществить полную репарацию.
Помимо этого группа занимается изучением роли специфических клеточных популяций в нормальном функционировании организма, например популяций тучных клеток и М2 макрофагов в узлах автоматии сердца млекопитающих.
Состав группы: с.н.с. кбн, Васильева Тамара Викторовна, н.с. Федоров Артем Валерьевич
Контакты группы: Васильева Тамара Викторовна vasilyev-n@yandex.ru, Федоров Артем Валерьевич +79852349487 mergon80@yandex.ru
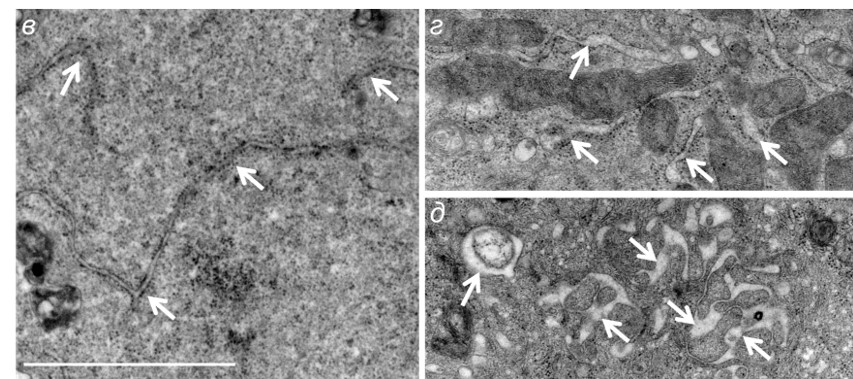
Активация стресса ЭПР в клетках НаСаТ и А431 при воздействии жасмоновой кислотой (ЖК). в–д – ЭПР в клетках НаСаТ при воздействии ЖК: в – контроль, г и д – ЖК; в–д – ТЭМ, стрелки указывают на цистерны ЭПР, масштабный отрезок – 2 мкм
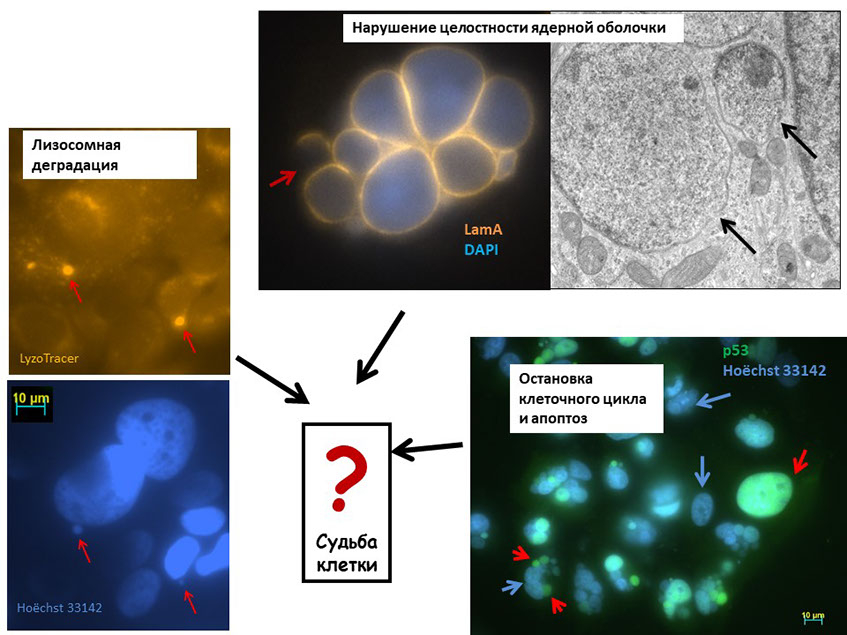
Изучение механизмов деградации микроядер в опухолевых клетках
Группа проф. Киреева И.И.
Тема: «Принципы ультраструктурной организации интерфазных и митотических хромосом»
Лаборатория реализует несколько проектов, направленных на изучение структурной организации интерфазного ядра и митотических хромосом в норме и патологии.
Группа занимается исследованием роли комплексов архитектурных белков хромосом когезина и конденсина в пострепликационной упаковке ДНК, интерфазной индивидуализации сестринских хроматид после репликации и динамики хроматиновых доменов при формировании митотических хромосом. Целью исследования также является выяснение механизмов, посредством которых когезин и конденин участвует в поддержании стабильности генома и регуляции экспрессии генов. В рамках проекта применяются современные методы молекулярной биологии и субдифракционной и электронной микроскопии. Полученные результаты могут предоставить новый взгляд на процессы, регулирующие 3D-структуру ядра и её роль в нормальном функционировании клеток, а также в развитии патологических состояний, таких как опухолевая прогрессия.
Другой проект посвящен изучению роли ядерной ламины в поддержании механических свойств ядра и ее роли в метастазировании рака. Ядерная ламина является важной структурой, обеспечивающей механическую стабильность ядра и регулирующей различные биологические процессы, включая геномную стабильность и экспрессию генов. Изменения в составе и структуре ядерной ламины могут приводить к нарушению механических свойств ядра, что, в свою очередь, может играть ключевую роль в процессах метастазирования раковых клеток. Целью проекта является выяснение механизмов, посредством которых изменения в ядерной ламине влияют на механические свойства ядра и способствуют метастазированию рака, а также в разработке терапевтических подходов для ингибирования метастазирования через регуляцию структуры ядерной ламины.
Подробнее информацию о работах группы можно найти в системе ИСТИНА МГУ: https://istina.msu.ru/workers/379155/
Контакты: iikireev@gmail.com - Киреев Игорь Игоревич
Антиподальные клетки зародышевого мешка пшеницы в ходе дифференцировки и программируемой клеточной гибели
Антиподальные клетки формируются до двойного оплодотворения и вскоре после него подвергаются гибели. У злаков антиподальные клетки сохраняются дольше, чем у других растений и формируют трехуровневый комплекс из 27-30 клеток, которые проходят раунды эндоредупликации, вследствие чего в их ядрах формируются политенные хромосомы. В ходе этапа дифференцировки антиподальные клетки питают развивающийся ценоцит эндосперма, а процесс целлюляризации (закладки клеточных стенок) запускает программируемую клеточную гибель антиподальных клеток. Онтогенез антиподальных клеток до сих пор слабо изучен. В рамках данной подтемы антиподальные клетки рассматриваются как пример растительных клеток с политенными хромосомами, изучается структура политенных хромосом, особенности их компактизации, изменение их структуры в ходе онтогенеза, структура и распределение органелл цитоплазмы антиподальных клеток и их изменение в ходе дифференцировки и программируемой клеточной гибели.
Состав погруппы: ст.н.с., к.б.н. Лазарева Елена Михайловна, н.с., к.б.н. Доронина Татьяна Валерьевна.
Контакты сотрудников: matveevatatiana.94@yandex.ru - Доронина Татьяна Валерьевна
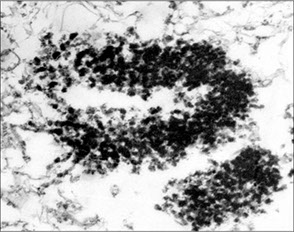
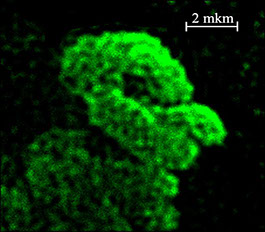
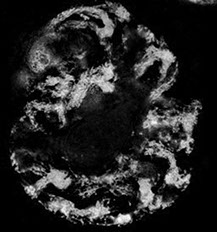
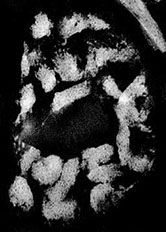
Хромосомы - ТЭМ и флуоресцентная микроскопия
Политенные хромосомы антиподальных клеток, флуоресцентная микроскопия.
Группа проф. Воробьева И.А.
Тема: «Роль цитоскелета в клеточной подвижности»
Группа занимается исследованием представленности и функций неканонических миозинов I класса и их изоформ в клетках различных тканей в норме и при патологии. Эти белки имеют сложную тканеспецифичную представленность, которая может изменяться при опухолевой трансформации клеток и, возможно, при смене их функционального состояния (активация, передача сигнала, миграция) в норме. Роль миозинов I класса в ремоделировании плазматической мембраны клеток при их движении и передаче сигналов от рецепторов не до конца изучена; способность некоторых изоформ данных белков локализоваться в ядре клетки позволяет также предположить у них дополнительные сигнальные функции, не связанные с плазматической мембраной.
Так, изоформа А миозина I C специфически гиперэкспрессируется при раке предстательной железы. Ряд работ группы был посвящен исследованию как биомаркерного потенциала этого белка при раке простаты, так и его механистическим функциям в опухолевых клетках.
В настоящее время работа группы сфокусирована на исследовании миозинов I класса в иммунных клетках, которые являются наиболее подвижными клетками в многоклеточном организме. При понимании решающей роли, которую имеет ремоделирование плазматической мембраны в процессе сигнальной активации и подвижности этих клеток, предполагается установить, какие именно из миозинов I класса преобладают в популяциях различных иммунных клеток человека, изменяется ли их состав при созревании и активации этих клеток, а также какой спектр функций закреплен за каждым из экспрессируемых миозинов I.
Состав группы: д.б.н., проф., Воробьев Иван Андреевич, к.б.н., в.н.с. Саидова Алина Александровна, к.б.н., в.н.с. Поташникова Дарья Марковна, м.н.с. Ковалева Анастасия Викторовна, учебный мастер Соломатина Евгения Сергеевна.
Контакты сотрудников: dariapotashnikova@yandex.ru – Поташникова Дарья Марковна.
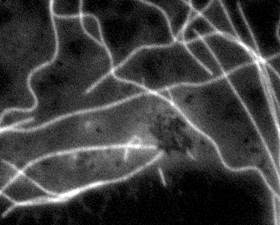
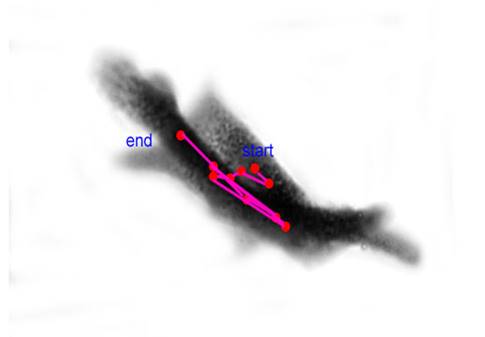
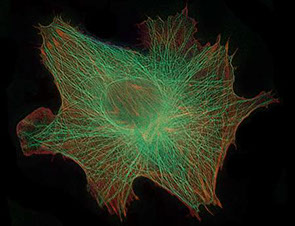
Коллаборация по исследованию морфологии и ультраморфологии атеросклеротических бляшек человека.
Целью коллаборации является анализ и обобщение имеющихся данных о факторах прогрессии и дестабилизации атеросклеротических бляшек человека, а также поиск морфологических и морфометрических параметров бляшек, наилучшим образом коррелирующих с рисками возникновения сердечно-сосудистых событий у пациентов. В настоящее время активно ведется поиск маркеров, ассоциированных с прогнозом, в том числе на уровне гистологической / иммуногистохимической детекции. Был выявлен ряд перспективных характеристик, потенциально имеющих прогностическое значение при атеросклерозе, таких как доля липидных включений и коллагеновых волокон в атеросклеротической бляшке, площадь некротического кора и толщина фиброзной покрышки над ним, наличие и доля очагов геморрагии и кальцификации в бляшке, доля иммунных клеток в бляшке и их популяционный состав. Однако консенсусного набора параметров и способов их оценки на данный момент нет. Сравнения полученных результатов с клиническими данными пациентов и показателями неинвазивных методик исследования (КТ / УЗИ) также были весьма ограниченными. Таким образом, качественное и количественное морфологическое и ультраморфологическое описание состава атеросклеротических бляшек человека после проведенной эндартерэктомии и сравнение полученных данных с клиническими характеристиками пациентов является актуальной задачей, позволяющей найти новые факторы риска, связанные с дестабилизацией бляшек и сопутствующими осложнениями при атеросклерозе.
Состав коллаборации на кафедре клеточной биологии и гистологии: к.б.н., доц. Липина Татьяна Владимировна, к.б.н., в.н.с. Поташникова Дарья Марковна.
Контакты сотрудников: tlipina@mail.ru – Липина Татьяна Владимировна. dariapotashnikova@yandex.ru – Поташникова Дарья Марковна.

%20(1).jpg?crc=4071970989)
Гладкий миоцит в атеросклеротической бляшке человека, ТЭМ
Телоцит, монтаж ТЭМ
Группа Е.В. Шеваля
Тема: «Клеточные и молекулярные основы биогенеза тканей в норме и патологии»
Основные интересы группы связаны с изучением механизмов биогенеза клеточных и тканевых структур в норме и при развитии патологий. В работе сочетаются вычислительные и экспериментальные подходы. В настоящее время работа ведется по трем направлениям:
1. Механизмы биогенеза клеточных органелл.
Многие клеточные органеллы не окружены мембранами, что, с одной стороны, позволяет им очень гибко реагировать на изменения внешних условий, но, с другой стороны, требует развития специальных механизмов для поддержания их структурной целостности. В настоящее время мы изучаем роль белков с природно неупорядоченными доменами в поддержании целостности и обеспечении лабильности безмембранных структур (ядрышки и стресс-гранулы).
2. Tat белок вируса иммунодефицита человека: механизмы патогенности и поиск новых антиретровирусных препаратов.
Tat вируса иммунодефицита человека (ВИЧ) необходим для активации вирусной транскрипции, а кроме того, способен выходить из инфицированных клеток и накапливаться в крови, вызывая различные ВИЧ-ассоциированные заболевания (например, лимфомы). В настоящее время работа с Tat белком ВИЧ ведется по двум направлениям. (1) Проводится изучение эволюции патогенности Tat белка у лентивирусов (с особым упором на возникновение ВИЧ-1). (2) Ведется создание тест-системы для поиска новых ингибиторов Tat белка, которые могут в дальнейшем использоваться в качестве антиретровирусных препаратов.
3. Морфологический и биоинформационный анализ процессов биогенеза нормальных и неопластических тканей.
Основным нашим интересом в этой области является изучение морфологии и функций новых или плохо охарактеризованных типов клеток. Также мы изучаем особенности стромы опухолей. Эта работа ведется с использованием клинического материала и преследует не только научные, но и диагностические цели.
Подробнее информацию о работах группы можно найти в системе ИСТИНА МГУ: https://istina.msu.ru/profile/sheval_e/
Контакты: Шеваль Е.В. sheval_e@belozersky.msu.ru
Научные связи кафедры в МГУ
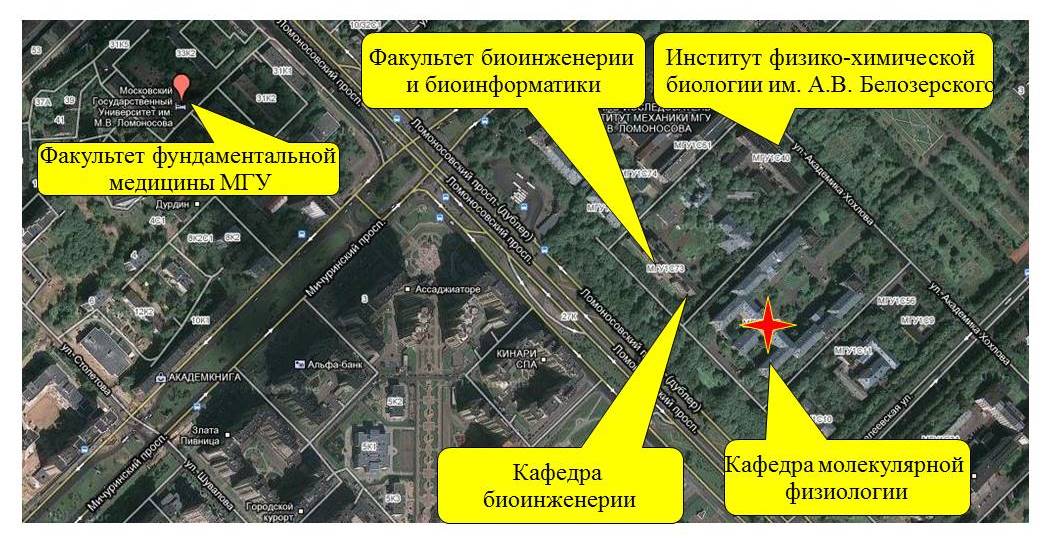
Научные связи кафедры в Москве
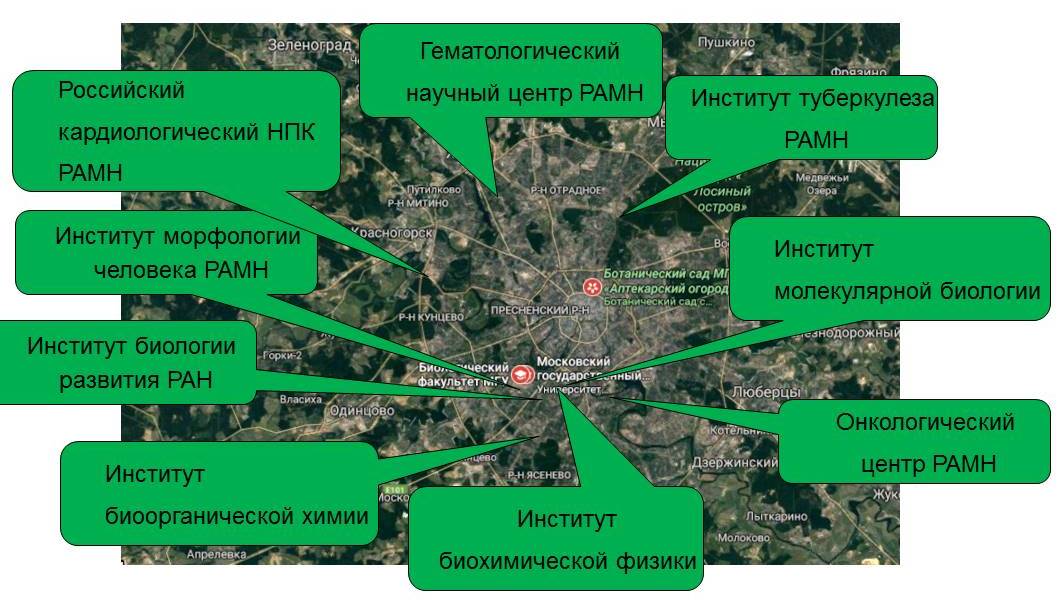
Кафедра молекулярной физиологии МГУ
Наверх ↑
Телефон:
8(495) 939-17-94
Электронная почта:
cellbiologymsu@yandex.ru
Адрес:
Ленинские Горы, д.1., стр.12, 3-й этаж, каб. 376